![]()
問1. IF4-:平面四角形,PF4-:シーソー形
問2. 中性分子XeO4, SO2F2など,1価陰イオンIO4-, ClO4- など
問3. CO32-:平面三角形,SOF2:三角錐
問4. 水素とハロゲンはこのような系ではいずれも1電子を中心原子と共有する.分子構造を決めているのは中心原子回りの電子数であると考えると問題文のような分子同士も等電子・等構造と考えてもよい.
問5. 2種類 (炭素原子が隣合ったものと対角線に向かいあったもの)
問6. 6-1)3種類
6-2)6-3)1,2 極性あり; 1,7 極性あり; 1,12 極性なし
![]()
問1. a (理由)枝分かれ部分での温度が実際に捕集される蒸気の温度であるため.
問2. 水の沸騰に伴う水蒸気発生用釜の内圧の変化を補償して(安全弁のはたらき),丸底フラスコへ供給する水蒸気の圧力を一定範囲に保つため(水蒸気の安定供給).
問3. P1/Pw
問4. P1 M1/Pw Mw
問5. アニリンには分子間水素結合があるがトルエンにはそれがないため.
問6. (作図省略)84 ℃
![]()
問1. シリカゲルには空孔があってそこに水が吸着されるが,ち密な石英にはそのような空孔がないため.
問2. 0.5(共有O) × 3 = 1.5, 1(非共有O) × 1 = 1 1.5 + 1 = 2.5 ∴2.5
問3. 12個
問4. Si/Al比2の方がAlの置換の程度が高く,それだけ電気的中性を保つNaイオンを多く含むので,Si/Al比3のゼオライトよりSi/Al比2のゼオライトの方が多くのCaイオンを除去できる.
問5. (A)塩酸などの酸
(B)塩化アンモニウム水溶液などのアンモニウムイオンを含む水溶液
![]()
問1 チオ硫酸イオン S2O32- :-2,四チオン酸イオン S4O62- :-1
問2 Na2CO3 + CO2 + H2O → 2 NaHCO3
問3 ヨウ素滴定では過剰のヨウ化カリウムの存在下で酸化還元反応を行う.このため,ヨウ化物イオンより酸化されにくい塩化物イオン(塩酸に由来)が酸化されることはない.
問4 2MnO4- + 16H+ + 10I- → 2Mn2+ + 5I2 + 8H2O
問5 H2O2 + 2H+ + 2I- → I2 + 2H2O
問6 2.96%
![]()
問1. 炭素数Nの増加に対して単調に,かつ滑らかに増加する.増加の割合は,Nに対して1次よりはわずかに小さい.
問2. 炭素数が同じ場合には枝分かれの度合いが大きいものほど沸点は低下する.
問3. 36℃
問4. (全部で8種)
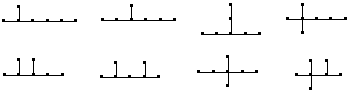
問5.
![]()
3-メチルヘキサン 2,3-ジメチルペンタン
![]()
問1. 1, 4, 5, 6, 8, 9
問2. 5, 6, 8, 9
問3. 5, 8, 9
問4. 5
日本化学会・化学教育協議会・平成11年度高校化学グランプリ小委員会(委員長:渡辺 正)
(ページ管理責任者:伊藤眞人:itomasa@t.soka.ac.jp)