注意事項
授業で用いるときは教員の指示に従うこと。
章(注意:「回」ではない)番号をクリックすると、その章の問題にジャンプできます。
1.有機化合物の概要
2.原子の電子構造と共有結合
3.飽和炭化水素
4.不飽和炭化水素
5.官能基とその性質
6.立体化学:立体配座
7.立体化学:立体配置と立体異性体
10.有機化学反応の分類と特徴(1)有機反応の概要だけを学んで終わる場合
10.4 有機化学反応の実例
1-3)置換反応と脱離反応(1)
4-5) 付加反応(1)
6) ベンゼン環の求電子置換反応(1)
(課題)最初の課題は「身近な有機物と無機物」です。初回ですので、これから学ぶ内容が、身の回りのどこにあるどのようなものと関係しているかを学びます。
進め方は次の通りです。
(1)予め、いろいろな物質名をできるだけ集めておく(教科書に書いてあるもの以外のものが望ましい)。成分表など(衣類、食品、文具その他の日用品、化粧品、浴用・清掃用品、市販薬などについている)、一般的な書籍などを参考にするとよい。
(2)集めた物質を、(A)有機物か無機物か、(B)金属、イオン性物質、分子性物質、高分子のいずれに該当するかに基づいて分類し、整理する。たとえば、下のような表を作り、該当欄に物質名を記入するとよい。なんとか見当をつける努力をするのは自分の自信になるが、まったく見当もつかない人はヒントを参照してよい。
|
|
|
|
| 金属 | (存在しない) | |
| 分子性物質 | ||
| イオン性物質 | ||
| 高分子物質 |
(ヒント)上表を作る前段階として、まず次のような下書きをするとよい。
物質名 有機物 無機物 金属 分子 イオン 高分子
(名称) (該当欄に○) (いずれか該当する欄に○)
(3)上記(2)のようにしてまとめた表(ヒントの下書きではない)を、レポートとして提出する(ヒントの「下書き」は提出不要)。
注意:次のようなものは誤答なので、回答しないように。
物体名:アルミ箔, 一円玉、カーボンファイバー、木,消しゴム、人体など。
集合名または状態名: 塩(えん),ガス(気体)など。
品名:酒、サプリメント、調味料、安定化剤、医薬品、果汁、紙など。
混合物:塩酸、エキス,コーヒー、石油(原油),ゼラチン,炭酸、炭素繊維強化プラスチック(CFRP)など。
1.次の記述にあてはまる原子またはイオンの化学式を答えよ。
(1) 原子番号が11の原子からできる安定な陽イオン
(2) 陽子数が16の原子からできる安定な陰イオン
(3) 中性では電子数が12の原子からできる安定な陽イオン
(4) 周期表で第2周期第18族の原子
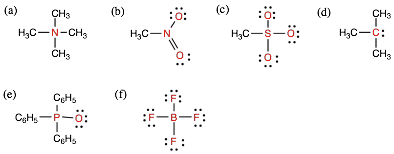
2.次の各分子を表す式で、―で示した結合は、極性のある共有結合、極性のない共有結合、イオン結合のどれにあてはまるか。
3.次の各電子式(Lewis構造式)について下の問いに答えなさい。
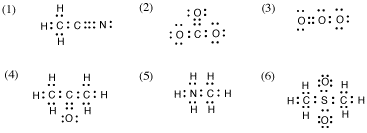
(a) 水素と炭素以外の原子の形式電荷をそれぞれ計算しなさい。
(b) それぞれどのような構造式と対応するか。電荷を含めて描きなさい。各構造式が表す化学種(分子、イオンなどの総称)の名前を調べてみよ。
5.次の電子配置で示される原子またはイオンの化学式を答えよ。
(1) 1s22s22p6 の一価陽イオン (2) 1s22s22p63s23p6 の二価陰イオン
(3) 1s22s22p6 の二価陽イオン (4)1s22s22p6 の中性原子
6.水素以外の原子の電子軌道に関する次の問いに答えなさい。
(1) 同じ名前の軌道(1s, 2s, 2pなどのいずれか一つ)の (a) エネルギー準位および (b) 原子核からの平均距離は、原子番号が大きくなると、それぞれどのように変化するか。理由と共に答えなさい。
(2) 同じ原子で同じ主量子数(n)の軌道(たとえば3sと3pと3d)のエネルギー準位の順序はどうなるか。理由と共に答えなさい。(注:水素原子では同じ主量子数の軌道のエネルギー準位は等しい。
以後の問いでは分子模型と分度器を用意すること。 Winmostarを使って描いてもよい。手元にない場合には参考書など書籍等の記述に基づいて想像して図を描き、答えるのもやむを得ない。
7.(分子模型)授業資料2-8ページ2.7の各分子の模型を作り、次の問に答えなさい。
丸善HGS模型を使用
(1) 授業資料2.7のメタンの模型を作りなさい。C原子には四面体用の黒いたまを、H原子には水色のたまを用い、C-H結合には2番の棒を用いなさい。資料の図のように置き、くさび形の線と点線の意味を確認しなさい。それぞれどのような方向を意味するか、自分の言葉で他人がわかるように説明しなさい。(2) 授業資料2.7のメタナール(ホルムアルデヒド)の分子模型を次の2通りの方法で作り、問いに答えなさい。O原子には赤色のたまを用いる。
(a) 四面体用のC原子のたまを用い、10番の曲がった棒2本で二重結合を表す。
(b) 三角形用のC原子のたま(四面体用より一回り大きい)を用い、4番または6番の棒で二重結合を表す。
それぞれについてH-C-HおよびH-C=Oのなす角を分度器で測り、どちらの模型が実際の角度により近いか答えなさい。(3) 二酸化炭素の分子模型を作りなさい。四面体用のC原子を用い、二重結合には(2)(a)と同様に10番の棒を用いる。模型の概要をスケッチしなさい(多面体のたまは球として、棒一本は一本の線で描いてよい。以下のスケッチの問題でも同じ)。
8.(高校化学の復習)次の分子式をもつ化合物のCとHの元素組成(質量パーセント)を求めなさい。原子量は小数第2位まで用い、答えは四捨五入して小数第1位まで求めること。
(1) C3H8 (2) C4H10 (3) C3H6 (4) C4H8
10-2.(希望者はこの問題にも取り組むとよい)元素組成の有効数字が整数まで(実験誤差がプラスマイナス0.5%)だとすると、元素組成だけから分子式をどこまで区別できるといえるか。上の結果から考えて見よ。
ヒント:まず、実験誤差を考えたときに上の(1)~(4)の分子式を互いに区別できるかを、元素分析の計算値をもとにして検討する。そして、炭素数が大きくなったときに元素分析の計算値の違いがどうなるかを類推して考察する。
このような考え方は、化学だけでなく、誤差を含む実験値を相互に比較する実験を行う分野では極めて重要である。
1(1)分子式がC6H14の炭化水素の異性体をすべて、構造式で描きなさい(構造が区別できれば、次の問題2の図のように簡略化された式で良い)。BIOVIA Draw で描き、MS Word ファイルに貼り付けてもいい。
(2) 1(1)で描いた各異性体にIUPAC名をつけなさい。
命名法プリントのルール[1]~[5][10]を参考にすること。
2(分子模型)(1)次の各構造式に対応する構造を分子模型で作り、どれとどれが同じ化合物を表すかを記号で示しなさい。
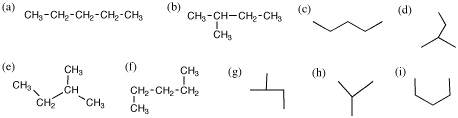
(2) 2(1)で得た分子のそれぞれに名前を付けなさい(同一の化合物には一つ記せば十分)。
---
次の問いは、3-3ページ「置換シクロアルカン類の異性体と命名法」を参考にしながら回答するとよい。
3.シクロヘキサン(C6H12)の構造異性体について次の各問いに答えなさい。立体異性体は区別しなくてよい。
(1) 1,1-ジメチルシクロブタンの構造式を描きなさい。
(2) (1)以外の四員環(原子4個からなる環)をもつ異性体の構造式をすべて描き、名前を答えなさい。
(3) 三員環をもつ異性体の構造式をすべて描き、名前を答えなさい。
4.次の各問いに答えなさい。
(1)~(4) 次の各環状飽和炭化水素の分子式を答え、IHD(水素不足指数、不飽和度)を求めなさい。
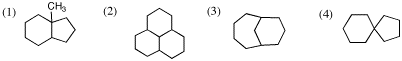
(5) 分子式がC17H28で、五員環または六員環だけをもつ環状飽和炭化水素の可能な異性体の構造を一つ答えなさい(側鎖はあってもなくてもよい)。(ヒント:まずIHDを求めると環の数がわかる)
命名法プリントのルール[6]~[9]を参考にすること。
補足:化合物名のうち、*は2013勧告に基づく推奨名(PIN,Preferred IUPAC Name)。以下同じ。1.(分子模型)(E)-2-ブテンおよび(Z)-2-ブテン(*ブタ-2-エン)の分子模型を作り、次の問いに答えなさい。二重結合を構成している炭素には三角形用のC原子のたま(四面体用より一回り大きい)を用いる。定規が必要。
(1) 各分子の模型の概略をスケッチしなさい。(模型が使えない場合は、(1) 授業資料その他の結合長・結合角のデータを基に概略を作画するか、(2)Winmostarで描いてペーストする。)
(2) (Z)-2-ブテンの両末端のメチル基の水素原子どうしが
(a) もっとも近づいた時と
(b) 最短距離がもっとも離れた時の、
両水素原子間の距離(各球の中心間の距離)をそれぞれ測りなさい。(丸善HGS模型では模型の1 cmは実際の0.04 nmと対応している。Winmostarでは、結合長を調べる方法と同様にして原子間距離を調べる)
(c) (b)の結果を、水素原子のvan der Waals半径0.12 nm(共有結合していない時、原子間距離がこの2倍より小さくなると、原子どうしはたがいに反発する)と比較すると、どのようなことが考えられるか、あなたの考えを答えなさい。
(3) (E)-2-ブテンおよび(Z)-2-ブテンではどちらがより安定だと考えられるか。(2) の結果に基づいて、理由とともに答えなさい。
2.分子式がC5H10の非環状炭化水素のすべての異性体を構造式で示し、それぞれにIUPAC名をつけなさい。
3.次の化合物の構造式を描きなさい。IHD(不飽和度)はそれぞれいくつか。
(注意:この設問が試験に現れたとき、IHDを答えなければ世間では100%問答無用で減点される。気をつけること。)
(1) cis-1,3-ペンタジエン、*cis-ペンタ-1,3-ジエン (2) 4-メチルシクロペンテン (3) 3-プロピル-1-ヘキセン、 *3-プロピルヘキサ-1-エン
(4) 1-オクテン-4-イン、*オクタ-1-エン-4-イン (5) (E)-2-ペンテン、* (E)-ペンタ-2-エン
4.次の各化合物の構造式中の共役系(共役二重結合でつながっている範囲)の部分を○で囲みなさい。
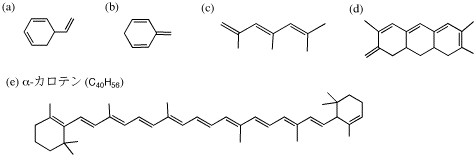
5.次の各化合物の構造式を答えなさい。
(a) シクロヘキシルベンゼン (b) 4-プロピルトルエン (c) 2-イソプロピルナフタレン (d) 4-フェニル-3-メチル-1-ブチン
6.ベンゼン環をもち、分子式がC9H12の化合物の異性体をすべて描き、それぞれに名前をつけなさい。
1.(分子の極性)次のうち (1)(2)(4)の各分子の模型を作り、それぞれ極性分子か無極性分子のいずれか答えなさい。ただし、C-H結合の極性は無視できるものとする。
2.次の各分子の模型を作り、次の各問いに答えなさい(丸善HGS模型ではNは青色、Oは赤色、Clは緑色の球をそれぞれ用いる)。
(a) CH3OH (b) CH3NH2 (c) CH2=O(Cはsp2用を用いる。丸善HGS模型の場合、二重結合は4番(ない場合は6番)の棒一本で表す) (d) CCl2=O((c) に同じ)
(1) 各模型の概略をスケッチしなさい(またはまとめて見やすく写真に撮り、回答用Wordファイルにペーストしなさい)。
アプリを用いる場合は、作成した画像の画面をコピーして回答用Wordファイルにペーストしなさい。(2) (a)と(b) ではどちらの分子のほうが極性が大きいと考えられるか。理由と共に答えなさい。
(3) (c)と(d) ではどちらの分子のほうが極性が大きいと考えられるか。理由と共に答えなさい。
(4) (a)と(c) ではどちらの分子のほうが極性が大きいと考えられるか。理由と共に答えなさい。
(ヒント)極性結合に関わる電子の数はどちらが多いか?また、σ結合の電子とπ結合の電子では、どちらが偏りやすいと考えられるか?
3.次の各化合物について、次の各問いに答えなさい。
(1) 各アルコールおよびアミンは、第一級、第二級、第三級および第四級アンモニウム塩のいずれであるかを答えなさい。
(2) 同一分子間で水素結合できないものはどれか((e)は除く) 。
化合物名に関する問題では「命名法プリント」を用いて回答する。
4.上の3.の各化合物に名前を付けなさい。講義資料「アミンの命名法への補足」を参考にすること。
(ヒント)(c) 慣用名では、(CH3)2CHCH2CH2-:イソペンチル(isopentyl)基または3-メチルブチル(3-methylbutyl)基を用いる。
(e) Et = CH3CH2。EtNH3Cl (Ethanammonium chloride、塩化エタンアンモニウム)のN-置換体として命名する。上記資料の(CH3CH2)3N を参考にする。
(f) C6H5NH2 がアニリンという慣用名で呼ばれることを利用する。
5.次の各化合物について以下の各問いに答えよ。*は「有機化学命名法IUPAC勧告2013(2013勧告)」に基づく推奨名(PIN,Preferred IUPAC Name)。以下同じ。
(a) 2-ブタンアミン (b) 2-ブタノール (c) プロパン酸 (d) 2-ブタノン
*((a) ブタン-2-アミン (b) ブタン-2-オール (c) プロパン酸 (d) ブタン-2-オン)
(1) (完全な)構造式を描け。
(2) (1)で描いた構造式中の水素結合に関与する水素原子(D)および水素受容原子(A)にそれぞれD、Aの記号をつけよ。
6.酢酸(エタン酸)の沸点が分子量に比べて高いのはなぜか?構造式を用いて説明せよ。
7.次の分子式に対応するIHD(水素不足数または不飽和度)を求めよ。中性分子として存在しうるものは、これまでに出てきた官能基のいずれか(1つ以上)を用いて、可能な構造式を一つ示せ。中性分子ではなく、基(または陽イオン、陰イオン)として存在しうるものは、可能な基(または陽イオン、陰イオン)の構造式を一つ示せ。また、単一の化学種としては存在し得ないものは、×で示せ。
(1) C5H14O2 (2) C2H5NO (3) C4H10N3O
(4) C6H5NO2 (5) C6H16N (6) C5H9Cl5
8.(元素組成・構造決定)ある有機化合物の元素分析を行ったところ,C: 42.87%,H: 2.40%,N: 16.66%で,残りは酸素だった。次の各問いに答えよ。
(1) この有機化合物の組成式を求めよ。
(2) この有機化合物の分子量が160~170の範囲である時,この化合物の分子式を求めよ。
(3) この化合物はベンゼン環をもち,ニトロ基以外の官能基をもたないことがわかった。この有機化合物の構造として考えられるものをすべて答えなさい。
(補足)元素分析により元素の化学組成(組成式)を求め、分子量のデータを加えて分子式を定める過程は化学にとって基本的に重要な内容であり、高校化学では有機化学の編の冒頭で必ず取り扱っています(無機化学でも当然必要。わからない人は復習して下さい)。ところが、マークシート方式の問題になじまないため、大学入試問題で出題されることはあまりありません。このためか、センター試験やマークシート試験対策しか考えていない学校では「入試に出ないから」といって、きちんと教えていない場合もあるようです。「きちんと習ってない」不運を嘆いても仕方ないので、教科書や参考書をひっくり返して、ちゃんとできるようになって下さい。
9.次の各化合物の構造式を沸点の低いと考えられるものから順に左から右に並べなさい。
(1) (a) 2-ブタノール (b) プロパン酸 (c) 2-ブタンアミン
*((a) ブタン-2-オール (b) プロパン酸 (c) ブタン-2-アミン)
(2) (a) 2-ブタノン (b) 2-メトキシプロパン (c) 2-メチルブタン
*((a) ブタン-2-オン (b) 2-メトキシプロパン (c) 2-メチルブタン)
10.次の各化合物の構造式を水溶性の低いと思われるものから順に左から右に並べなさい。
(1) (a) 2,3-ジメチルブタン (b) 3-メチル-2-ブタノン(メチルイソプロピルケトン) (c) 3-メチル-2-ブタノール
*((a) 2,3-ジメチルブタン (b) 3-メチルブタン-2-オン (c) 3-メチルブタン-2-オール)
(2) (a) 1,3-プロパンジオール(プロピレングリコール) (b) 1-ブタノール (c) エトキシエタン(ジエチルエーテル)
*((a) プロパン-1,3-ジオール (b) ブタン-1-オール (c) エトキシエタン)
11.次の各化合物の構造式を、酸性の弱いものから順に左から右に並べ、理由を簡単に説明しなさい。(「化学B」では
理由を正しく答えられなくてもいいが、学んできた範囲で答えるよう努力する。)
注意:「pKaが大きい(小さい)から」という回答は「同義反復」であり、「理由」を述べたことにはならない。
cyclohexanol phenol cyclohexanecarboxylic acid
12.次の各化合物の構造式を、塩基性の弱いものから順に左から右に並べ、理由を簡単に説明しなさい。(「化学B」では理由を正しく答えられなくてもいいが、学んできた範囲で答えるよう努力する。)
1-hexanamine aniline (benzenamine) hexanamide
*(hexan-1-amine aniline (benzenamine) hexanamide)
13.次の各問いに答えなさい。
(1) プリント5-13ページ、「5.11 構造異性体」の(2)のC4H6の異性体は描いたもの以外にもいくつかある。すべてを構造式で答えよ。
(2) プリント5-13ページ、「5.11 構造異性体」の(4)3)の(補足)に該当する異性体の構造を、重複のないように描けるだけ描いてみよ。ただし、C=C-OH(エノール)という部分構造をもつものは除外すること(多くなりすぎるし、一般に不安定なため)。
14.(元素組成と官能基・異性体)次の化学式で表される化学種の元素組成(質量百分率で小数第2位まで)を求めよ。そして,与えられた条件をみたす物質の構造をすべて構造式で答えよ。
(a) C5H12O2 炭素骨格に枝分かれはなく,OH,O-O,O-C-O はない。
(b) C4H10N2 炭素原子はすべてsp3混成であり,環はなく,N-Hはない。
(c) C6H6SO3 一置換ベンゼンで,O-Oはない。
(d) C6H16NCl イオン性物質(塩化物塩)である。同じアルキル基が2つ以上あり,C-ClやN-Clはない。
1.2,4-ヘプタジエン(*ヘプタ-2,4-ジエン)には何通りのシス・トランス異性体があるか。すべてを構造式で(異性体を区別できるように)描きなさい。
2.(分子模型)1,2-ジクロロエタンの分子模型を作り、C-C結合のまわりで回転させてできる安定な配座異性体をNewman投影図で描きなさい(ヒント:3つある)。それぞれの異性体のねじれ角を示しなさい。
3.(分子模型)シクロヘキサンの分子模型を組んで、次の問に答えなさい。
(1) いす形の構造を作り、スケッチしなさい。6本のC-C結合の立体配座に注目しなさい。ねじれ形のものがいくつ、重なり形のものがいくつあるか。
(2) 舟(ボート)形の構造を作り、スケッチしなさい。6本のC-C結合の立体配座は、ねじれ形のものがいくつ、重なり形のものがいくつあるか。
4.「有機化学I・演習問題」にある演習問題を開く(第1集)(pdfファイル)をダウンロードし、第7章の[2]を解きなさい。
5.(分子模型)メチルシクロヘキサンの安定な配座異性体の分子模型を作り、スケッチしなさい。アキシャル位にある水素のそばに"ax"と記しなさい。アキシャル位の水素とエカトリアル位の水素はそれぞれ何個ずつあるか。
6.(任意課題)27 ℃で平衡状態にあるとき、シクロヘキサンのねじれ舟形の割合はイス形のおよそ何%か(有効数字2桁)。配座エネルギ-は6-4ページの図の値を用いよ。
ヒント:6-3ページの「補足」にある式を用いる。
1.「有機化合物の命名法」補習問題に答えなさい。
7.次の各化合物の構造式を描きなさい。考えられる立体異性体をそれぞれくさびと点線を用いて描き、不斉炭素原子があれば絶対配置(RかSか)を答えなさい。
(1) 2-pentanol (*pentan-2-ol) (2) 3-pentanol (*pentan-3-ol) (3) 2-hydroxypropanoic acid
8.(分子模型)次の各化合物の分子模型をつくりなさい。塩素は緑色、臭素は赤色の球を用いなさい。
(a) (R)-1-bromo-1-chloroethane (b) (S)-3-methoxy-2-butanone (*(S)-3-methoxybutan-2-one)
(c) (2R,3R)-3-chloro-2-butanol (d) (2S,3R)-3-chloro-2-butanol
*((c), (d)は立体化学を別にすると共に3-chlorobutan-2-ol)
(1) 立体構造がわかるように分子模型をスケッチしなさい。
(2) 構造式を、くさびと点線を用いて立体構造がわかるように描きなさい。
(3) (c)と(d) は互いに鏡像の関係かどうか、分子模型でチェックしなさい。
9.不斉炭素原子を持つ鎖状飽和炭化水素で、炭素数がもっとも小さいものの構造式を、くさびと点線を用いて立体構造がわかるように描きなさい。描いた化合物に、絶対配置(RかSか)を含めて名前をつけなさい。
10.次の問いに答えなさい。ただし,旋光度を測定するためのセルの長さは全て10 cm(1 dm)とし,ナトリウムランプ(D
線)を用いて測定したとする。
(1) 1.0 g の(S)-グルタミン酸モノナトリウムの10 mL 水溶液を作り,旋光度(θ)を測ったところ,+2.52°だった。(S)-グルタミン酸モノナトリウムの比旋光度
[α]D はいくらか。
(2) (1)のとき,1.0 g の(R)-グルタミン酸モノナトリウムの5 mL 水溶液の旋光度(θ)はいくらになるか。
11.(Fischer投影式) 上の問7(1)~(3)および問8(a)~(d)の化合物の立体構造を、Fischer投影式で記しなさい。
12.次の問題を解きなさい。
(「有機化学I・演習問題 第1集」の第6章「立体化学:立体配座と立体異性体」の[5]と同じ問題)
「絶対配置を答える」とは、不斉炭素原子の立体配置が R または
S のどちらであるかを答えることである。
13.(分子模型)シクロヘキサンの水素原子のうち二個を塩素原子(通常は緑色の球を用いる)で置き換えたときに生じる異性体を考えられるだけ、イス型配座でスケッチしなさい。塩素原子のうち1個を同じ位置に置いてスケッチすると、同一か違うかが区別しやすい。
(ヒント)立体異性体を区別しなければ4通り。cis-trans異性体(ジアステレオ異性体)を区別すれば7通り。鏡像異性体も区別すれば9通りになる。うっかり環反転による立体配座(異性体には含めない)を区別して描くと14通りになってしまう。
1.次の各反応はいずれも高校の教科書に載るほどよく知られている。示性式または簡略化された構造式を用いてそれぞれを完全な(物質収支の合った)化学反応式で表し、「物質レベルの分類」に従って反応の種類を答えなさい。
(1) エタノールと酢酸から酢酸エチルが生成する。
(2) アセチレン(HC≡CH)と酢酸から酢酸ビニル(CH2=CHOCOCH3)が生成する。
(3) エタノールを酸触媒の存在下で加熱するとエチレンが生成する。
(4) α-グルコースを水に溶かすと、一部がβ-グルコースになる。
(5) アセトアニリドに濃硝酸を作用させるとp-ニトロアセトアニリドが生成する。
2.次の各問いに答えなさい。原子量は小数第二位まで用いて計算すること。
(1) エタノールと酢酸から酢酸エチルができる反応を化学反応式で書きなさい。
(2) エタノール25 g と酢酸30 g から酢酸エチルを合成する時,仮に反応が完全に進行した(収率100%)とすると,生成する酢酸エチルは何mol
か。また,何g か。(「化学反応学」では、これを「理論収量」または「理論量」という。)
(3) (2) の条件で実際に反応を行ったところ,得られた酢酸エチルは27 g だった。酢酸エチルの収率は何%か。
(4) エタノール23 g と酢酸45 g を反応させて,22 g の酢酸エチルを得た。このとき酢酸エチルの収率は何%か。
3.次の各化合物の構造式を描き、求核種(または塩基)および求電子種(または酸)が接近しやすいと考えられる原子を、テキストの例にならって示しなさい。
(1) propene (2) benzoic acid (benzenecarboxylic acid, C7H6O2)
(3) 1-bromobutane (4) aniline (benzenamine)
(5) cyclohexanone (C6H10O) (6) ethyl acetate (ethyl ethanoate, C4H8O2)
4.有機化学反応では、同じ反応物(1つ以上)から、2組以上の生成物(1つ以上)が生じ、反応条件(温度など)によって主生成物(多く生じる生成物)が変わる場合がある。このような例を一つ挙げ、化学反応式を用いながら簡単に説明しなさい。
10.4 有機化学反応の実例
1.次の各反応の主生成物の構造を示し、名前を答えなさい。各反応の求核種と脱離基をそれぞれ示しなさい。
(1) ヨードメタンにナトリウムエトキシド(CH3CH2ONa)を作用させる。
(2) 1-ブタノール(*ブタン-1-オール)に硫酸酸性下で臭化水素を作用させる。
(3) 2-ヨード-2-メチルプロパンに、氷冷下で水酸化ナトリウム水溶液を作用させる。
2.次の各反応を化学反応式を用いて表しなさい。
(1) 塩化アセチル(塩化エタノイル、CH3COCl)と安息香酸ナトリウム(ベンゼンカルボン酸ナトリウム、C6H5COONa)を反応させる。
(2) N-エチルベンズアミド(C6H5CONHC2H5)を塩酸水溶液中で加水分解する。
3.主な求核種(あるいは求核種を生じる物質の組み合わせ)を1.に現れるもの以外に3つ挙げ、それぞれの関わる反応の具体的な例を一つずつ示しなさい。
4.次の各問いに答えなさい。
(1) 3-クロロ-2-メチルペンタンの構造式を描き、この化合物の脱離反応で考えられる生成物(有機物)をすべて答えなさい。
(2) 水酸化N-エチル-N,N-ジメチルプロパン-1-アンモニウム*の構造式を描き、この化合物の脱離反応で考えられる生成物(有機物)をすべて答えなさい。位置番号の"N"は、置換基がN原子に結合していることを示す。
*別名:水酸化N-エチル-N,N-ジメチルプロピルアンモニウム
1.次の反応の主生成物の構造を示し、名前を答えなさい。
(1) シクロペンテンに臭化水素を作用させる。
(2) 1,2-ジメチルシクロペンテンにPt触媒の存在下で水素を作用させる。
2.(E)-2-ブテン(*(E)-ブト-2-エン, (E)-but-2-ene、以下同様)に塩素を求電子付加反応させたときの主生成物(trans付加)の立体異性体を考える。
(1) (E)-2-ブテンの分子模型を作りなさい。C原子には三角形用のたまを用い、6番の棒一本で二重結合を示しなさい。
(2) (1)で作った模型を見ながら、付加反応で考えられる主生成物の立体構造をすべて分子模型で作り、必要に応じてくさびと点線を用いてスケッチしなさい。Cl原子には赤色または緑色の球を用いなさい。
(3) (2)でつくった各模型に対応する生成物に名前をつけなさい。
3.次の各反応の生成物を答えなさい。
(1) シクロヘキサノンに水中でシアン化ナトリウムを反応させる。もっとも安定な配座異性体を答えなさい。
(2) 2-ブタノン(*ブタン-2-オン)に塩化水素を反応させる。考えられる立体異性体の立体化学がわかるように描き、各不斉炭素原子の絶対配置(RかSか)も答えなさい。
1.ベンゼンの求電子置換反応の例を挙げ、それぞれで用いられる主な求電子種の発生法を化学反応式で示しなさい。
2.次の各化合物に硝酸と硫酸の混合物を作用させてモノニトロ化したとき、生成する異性体をすべて答えなさい。ただし、置換基による反応性や配向性の違いは考慮しないものとする。
(1) トルエン(メチルベンゼン) (2) m-キシレン(1,3-ジメチルベンゼン) (3) 2-クロロトルエン(1-クロロ-2-メチルベンゼン)
1.「有機化合物の命名法」補習問題に答えなさい。
2.「有機化学反応の基礎」の補習問題に答えなさい。